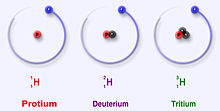
A hidrogénnek három fő izotópja van: a protium (1H), a deutérium (2H) és a trícium (3H). Ezek az izotópok abban különböznek egymástól, hogy hány neutron található az atommagban: a protiumnak nincs neutronja (csak egy proton), a deutériumnak egy neutronja van, a tríciumnak pedig két neutronja. A protium és a deutérium stabil izotópok, míg a trícium radioaktív — felezési ideje körülbelül 12,32 év — és bétabomlással visszaalakul 3He-vá.
Nevek és jelölések
A hidrogén fő izotópjai különlegesek abban is, hogy saját nevük van: protium, deutérium és trícium. A deutériumot és a tríciumot gyakran rövidítik D-vel és T-vel; ezek a jelölések széles körben használatosak a gyakorlatban. A Nemzetközi Tiszta és Alkalmazott Kémiai Unió (IUPAC) azonban hivatalos, formális kontextusban előnyben részesíti a tömegszámos jelölést (2H, 3H), bár a D és T megnevezések nem tűntek el a szakirodalomból.
Fizikai és kémiai következmények
A neutronszám különbsége a tömegekben és így a mozgási tulajdonságokban is jelentkezik, ami kémiai viselkedésre is hatással van. A deutérium tömege majdnem kétszerese a protiumének, ez:
- izotópikus eltolódást eredményez a spektrumokban (pl. infravörös rezgések),
- kinetikai izotóphatást okoz — kémiai reakciókban a kötésbontás lassabb lehet deutériummal, ezért a deutériumot mechanizmusvizsgálatokhoz és farmakokinetikai kutatásokhoz használják,
- a deutériummal képzett nehézvíz (D2O) fizikai tulajdonságai eltérnek a sima vízétől (pl. olvadáspont és forráspont eltérései), és különleges szerepe van nukleáris technológiákban.
Előfordulás és előállítás
A természetes hidrogén legnagyobb része protium: a földi vizekben a deutérium aránya kis töredék, körülbelül 150–160 ppm (0,015–0,016%). A trícium természetes mennyisége rendkívül alacsony; emellett kozmikus sugárzás és légköri folyamatok is létrehoznak nyomnyi tríciumot. Az ipari és kutatási célokra deutériumot és tríciumot különböző módszerekkel állítanak elő:
- deutériumot általában a víz elektrolízisével vagy lepárlással dúsítanak, így nyerik a nehézvizet (D2O),
- tríciumot elsősorban nukleáris reaktorokban vagy részecskegyorsítókban állítják elő neutronbefogással és más nukleáris reakciókkal; a trícium forrásai lehetnek továbbá nukleáris fegyverpróbák és bizonyos ipari tevékenységek.
Felhasználások
A hidrogénizotópok számos gyakorlati területen fontosak:
- Deutérium (D, 2H): neutronmoderátorként és hűtőközegként a nehézvizes reaktorokban (pl. CANDU); izotópdúsító anyagként és tracerként kémiai és biokémiai kutatásokban; NMR- és spektroszkópiai alkalmazásokban (oldószerként deutériált oldószereket használnak).
- Trícium (T, 3H): radioaktív tracerként biológiai és környezeti vizsgálatokban; önvilágító eszközökben (kis fényforrások, jelölők) speciális, zárt tartályokban; potenciális fúziós üzemanyagként (DT-reakciók, ahol deutérium és trícium egyesülve nagy energiát adnak).
- Protium (1H): minden „hagyományos” víz és szerves vegyület alkotóeleme, alapvető szereplő a kémiai és biológiai folyamatokban.
Biztonság és környezeti vonatkozások
A trícium radioaktivitása miatt kezelése, tárolása és kibocsátása szigorú szabályozás alá esik. A trícium béta-sugárzása alacsa energiájú, így külső sugárzásként általában kevésbé veszélyes, de belélegzés, lenyelés vagy bőrön át történő felvétel esetén belső sugárterhelést okozhat. A nehézvíz kémiai értelemben nem mérgező kis koncentrációban, de biológiai rendszerekben a hidrogén helyettesítése nagy arányban hatással lehet az élőlények működésére.
Mesterséges, rövid élettartamú izotópok
A tudósok további hidrogénizotópokat is előállítottak: 4H–7H. Ezek rendkívül instabilak, nagyon rövid felezési időkkel rendelkeznek, és a természetben nem találhatók meg; jellemzően gyorsan szétesnek neutronkibocsátással vagy más bomlási módokkal. Ezeknek az izotópoknak elsősorban alapkutatási jelentőségük van a nukleáris szerkezet és erős kölcsönhatások vizsgálatában.
A hidrogén izotópjai tehát nemcsak alapvető tudományos érdeklődés tárgyai, hanem fontos gyakorlati szerepet is betöltenek az energiatermelésben, a kutatásban és ipari alkalmazásokban.